我院赵萌教授团队报道亮氨酸抑制自噬清除耐药白血病干细胞
急性髓系白血病(Acute myeloid leukemia,AML)是成人中最常见的恶性血液系统疾病之一,在目前的常规化疗和靶向药物治疗下,其五年生存率仍然低于50%。白血病干细胞(Leukemia stem cell,LSC)的化疗耐药是导致AML复发难治的主要原因。近年来研究发现细胞代谢对AML化疗耐药有重要调控作用。研究发现耐药AML细胞具有较高的细胞氧化磷酸化水平,抑制细胞氧化磷酸化可增强化疗药物对AML的治疗效果。同时细胞脂肪酸代谢也可以通过参与氧化磷酸化调控LSC的化疗耐药。近期研究发现氨基酸代谢也参与了LSC的化疗耐药。如:初发病人的LSC依赖氨酸代谢进行氧化磷酸化促进化疗耐药,复发病人的LSC则通过脂代谢代偿氨基酸代谢参与氧化磷酸化促进化疗耐药。同时,烟酰胺代谢也可以代偿氨基酸代谢,在BCL-2抑制剂维奈托克的耐药中发挥重要作用。此外,不同的氨基酸在白血病耐药中发挥了不同的作用,如:丝氨酸合成对FLT3-ITD+的AML细胞化疗耐药有重要调控作用。本课题组前期也发现,苯丙氨酸可以通过调控骨髓免疫微环境参与白血病的化疗耐药(https://mp.weixin.qq.com/s/8rzwfmRd3jP3xGH4swRRMg)。因此,研究氨基酸代谢对LSC化疗耐药的调控机制并开发靶向治疗策略具有重要意义。
2022年3月17日,我院赵萌教授联合蒋琳加研究员、吴钧教授带领的团队在Haematologica杂志(IF=9.94)上发表了文章A self-assembled leucine polymer sensitizes leukemic stem cells to chemotherapy by inhibiting autophagy in acute myeloid leukemia,研究团队系统性的研究了AML细胞中LSC通过增加细胞自噬抵抗化疗药物杀伤的分子机制,并发现补充亮氨酸可有效激活mTOR信号通路抑制细胞自噬,进而增强化疗药物对耐药LSC的杀伤作用。在此基础上该团队开发了新型药物亮氨酸阿霉素,可有效清除耐药LSC,延长白血病小鼠的生存期,该药物有望成为一种靶向细胞代谢的新型白血病治疗药物。
本研究中,研究团队通过小鼠耐药白血病细胞的单细胞测序结合临床AML病人数据的分析发现,化疗耐药AML细胞中mTOR通路被抑制而细胞自噬通路显著激活。通过进一步功能验证发现耐药LSC中mTOR通路被抑制但细胞自噬显著增强,研究者发现自噬抑制剂氯喹可有效抑制LSC的细胞自噬进而增强化疗药物对LSC的杀伤作用。由于氯喹的毒副作用和非靶向性导致其不适宜作为白血病自噬的靶向治疗药物,研究团队因此进一步开发了新型的氨基酸药物来抑制LSC的细胞自噬。亮氨酸可有效激活mTOR通路抑制细胞自噬的发生,在此基础上,研究者将亮氨酸设计并合成为可以体内给药的亮氨酸聚合物,并加载化疗药物阿霉素后成为新型的亮氨酸阿霉素。研究者在AML白血病小鼠的体内研究中进一步证实,相对于对LSC有富集作用的传统化疗,亮氨酸阿霉素可有效清除白血病小鼠体内的LSC,显著延长AML小鼠生存周期。
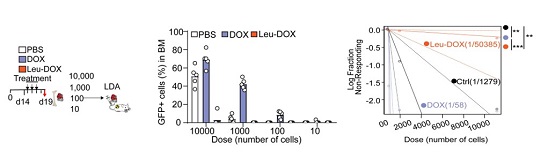
图1:亮氨酸阿霉素清除耐药白血病干细胞
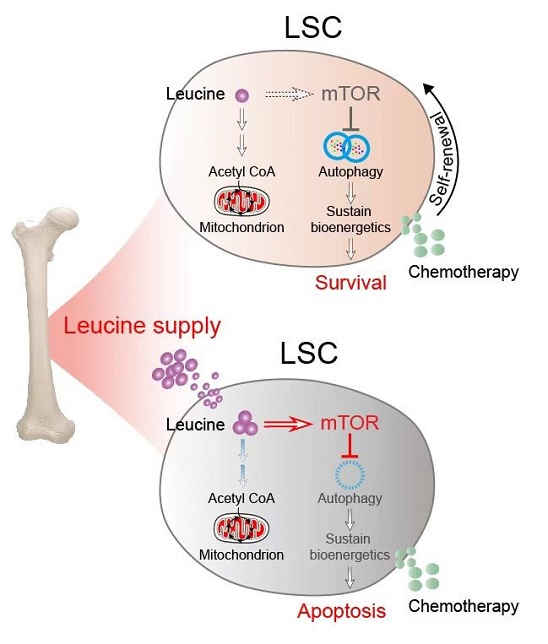
图2:亮氨酸抑制自噬提高LSC化疗敏感性
与本团队之前报道的结果类似,氨基酸化疗药物在体内可有效的靶向白血病细胞,但不影响正常血液细胞和造血干祖细胞,因此大大降低了化疗药物的骨髓抑制以及心脏和肾脏毒副作用。
综上,本研究证实亮氨酸可通过激活mTOR通路抑制LSC细胞自噬来增加化疗药物对LSC的杀伤作用,并开发了亮氨酸阿霉素可用于AML的治疗。本论文相关研究成果已经申请专利,并将开展后续的药物研发工作。本课题组还在进一步深入研究,亮氨酸代谢异常导致白血病化疗耐药的骨髓微环境和细胞内分子机制,为深入了解白血病化疗耐药机制提供新的研究思路。
中山大学的赵萌教授、蒋琳加研究员和吴钧教授为本文的共同通讯作者。徐曦博士、王健医生和仝彤博士为本文的共同第一作者。本项目得到了面上项目、干细胞重点研发项目和中山大学中山医学院-附属第一医院先进医学科学技术研究中心的支持。
原文链接:https://haematologica.org/article/view/haematol.2021.280290
(稿件来源:赵萌教授团队,初审:张晓红,审核:周家国,审核发布:张琪)



